ÇÖZÜNÜRLÜĞE ETKİ EDEN FAKTÖRLER
|
|
|
- Göker Armağan
- 7 yıl önce
- İzleme sayısı:
Transkript
1 ÇÖZÜNÜRLÜĞE ETKİ EDEN FAKTÖRLER 1- SICAKLIK 2- ORTAK İYON ETKİSİ 3- ÇÖZÜCÜ ÇÖZÜNEN CİNSİ 4- BASINCIN ETKİSİ 1- SICAKLIK ETKİSİ Sıcaklık etkisi Le Chatelier prensibine bağlı olarak yorumlanır. ENDOTERMİK ÇÖZÜNME : Isı + XY 2 (k) X +2 SUDA + 2Y -2 SUDA SICAKLIK ARTIRILIRSA : Denge ürünler tarafına kayar. XY 2 katısının çözünürlüğü artar. T artar Kçç artar. X +2 ve Y -1 iyon derişimleri artar. İletkenlik iyon derişimine bağlı olarak artar. XY 2 katısının kütlesi azalır. 1 yönündeki tepkime hızı daha fazla artar. Çözelti kütlesi artar. Çözelti yoğunluğu artar. SICAKLIK AZALTILIRSA: Isı + XY 2 (k) X +2 (SUDA) + Y -1 (SUDA) Denge girenler tarafına kayar. XY 2 katısının çözünürlüğü azalır T azalır Kçç azalır. X +2 ve Y -1 iyon derişimleri azalır. İletkenlik azalır. XY 2 katısının kütlesi artar. Çözeltisi yoğunluğu azalır. Çözelti kütlesi azalır. 1
2 EKZOTERMİK ÇÖZÜNME: XY (k) X +2 SUDA + Y -2 SUDA + ısı SICAKLIK ARTILIRSA: XY katısı kütlesi artar. Denge girenlere kayar. T artar Kçç azalır. XY katısının çözünürlüğü azalır. X +2 Y -2 iyon derişimi azalır. İletkenlik azalır. SICAKLIK AZALTILIRSA: Denge ürünler tarafına kayar. XY katısı kütlesi azalır. T azalır Kçç artar. XY katısının çözünürlüğü artar. X +2 ve Y -2 iyon derişimi artar. İletkenlik artar. NOT Gazların suda çözünmesi ekzotermik bir olaydır. O 2(g) O 2(s) + ısı Sıcaklık arttıkça gazların çözünürlüğü azalır. Balıkların soğuk suda daha iyi yaşamalarının sebebi budur. Kolayı soğuk içmemizdeki neden budur. 2
3 2- ORTAK İYON ETKİSİ Doymuş bir çözeltiye çözeltide bulunan iyonlardan bir tanesinin ilave edilmesi çözünürlüğü azaltır. AgNO 3 ilavesi AgNO 3 ilave Ag + Cl - AgCl (k) Ag + (s) + Cl - (s) AgCl (k) derişim * Ag iyonlarının derişimi artırır. * Çözünürlük azalır. [Ag + ] * Denge girenler tarafına kayar. * AgCl katı kütlesi artar. Ag Cl * Cl iyon derişimi azalır. [Cl - ] * Kçç değişmez. zaman NOT ORTAK İYON ETKİSİ SUDA AZ ÇÖZÜNEN TUZLARIN ÇÖZÜNÜRLÜĞÜNÜ AZALTIR ÖRNEK: a) 0,2 m lık NaBr çözeltisinde AgBr çözünürlüğü kaç mol \ l dir? b) AgBr saf sudaki çözünürlüğü kaç mol\l dir?(kçç= ) 3
4 ÖRNEK: Mg(OH) 2 katısı aşağıdaki eşit derişimli ve eşit hacimli sulu çözeltilerin hangisinde en az çözünür? A- Mg(NO 3 ) 2 B- NaOH C- MgSO 4 D- Ca(OH) 2 E- MgCl 2 3-YABANCI İYON (TUZ) ETKİSİ Çözünürlüğü az olan bir madde ortak iyon içermeyen bir elektrolit ortamında saf sudakine oranla daha çok çözünür. Aşağıdaki grafikte ortak iyon ve yabancı iyonun çözünürlüğe etkisi gösterilmiştir. Ag 2 CrO 4 çözünürlüğü KNO 3 etkisi K 2 CrO 4 etkisi Eklenen tuzun derişimi 4-BASINÇ ETKİSİ Dış basınç katı sıvıların çözünürlüğüne etki etmez. Basınç arttıkça gazların sudaki çözünürlüğü artar. 4
5 PH ETKİSİ Mg(OH) 2, Al(OH) 3.. bileşiklerde Ortama asit ilavesi yapılırsa : Al(OH) 3 Al OH - Denge ürünlere kayar. POH artar ph azalır OH azalır H artar. Çözünürlük artar. Kçç değişmez. ÇÖKELTİ OLUŞUMU- ÇÖKELME ŞARTI Pb(NO 3 ) 2 çözeltisi + NaI çözeltisi karıştırılırsa; Na + NO 3 - PbI 2 (k) Pb(NO 3 ) 2(K) Pb +2 (s) + 2NO 3 - (S) NaI (k) Na + (s) + I - (s) PbI 2 çöker 5
6 ÇÖKELME ŞARTI KÇÇ= Dengedeki bir sistemde iyonlar derişimi çarpımı. QÇÇ=İyonların denge derişimleri değil başlangıçtaki iyonların derişimleri çarpımıdır. İKİ ELEKTROLİT ÇÖZELTİ KARIŞTIRILDIĞINDA ÜÇ DURUM SÖZ KONUSUDUR!!! 1- QÇÇ= KÇÇ İSE ÇÖZELTİ DOYMUŞTUR. SİSTEM DENGEDEDİR. 2- QÇÇ KÇÇ DEN BÜYÜKSE ÇÖZELTİ AŞIRI DOYMUŞ ÇÖKELTİ OLUŞMAYA BAŞLAMIŞTIR QÇÇ KÇÇ DEN KÜÇÜKSE ÇÖZELTİ DOYMAMIŞTIR. ÖRNEK: 800 ML 0,04 M NaF çözeltisi ile 800 ML Pb(NO 3 ) 2 çözeltisi karıştırılıyor. Çökmenin olabilmesi için Pb(NO 3 ) 2 çözeltisinin derişimi en az kaç M olmalıdır? 6
7 ÖRNEK: K 2 CO L Mg(NO 3 ) 2 20 C 2L 20 C Aynı sıcaklık ve hacimde hazırlanan yukarıdaki çözeltiler karıştırıldığında çökme olmaması için K 2 CO 3 çözeltisinin derişimi en fazla kaç M olmalıdır? ÖRNEK: 0,3 M 400 ml K 2 CO 3 çözeltisiyle 1,2 m 400 ml HgCl çözeltisi karıştırılıyor. Çökme tamamlandıktan sonra çözeltide CO 3-2 iyonları molar derişimi kaç M olur? 7
8 ÖRNEK: Eşit hacimlerde M Ba(NO 3 ) 2 ile M NaF çözeltileri karıştırılıyor çökme tamamlandıktan sonra F - iyonları derişimi molar olduğuna göre BaF 2 çözünürlük çarpımı nedir? ÖRNEK: 0,1 M K 2 SO 4 çözeltisi ile 0,1 M BaCl 2 eşit hacimde karıştırılıyorlar çökelmeden sonra çözeltideki Ba +2 ve SO 4-2 iyon derişimleri kaçar M dır? 8
9 ÖRNEK: 100 ML M Ca(NO 3 ) 2 çözeltisi ile 100ml M NaF çözeltileri karıştırıldığında oluşan yeni çözelti CaF 2 ye doymuş hale gelmektedir CaF 2 nin çözünürlük çarpımı kaçtır? ÖNEMLİ: KATISIYLA DENGEDE OLAN BİR TUZ ÇÖZELTİSİNE SU EKLENİRSE; CaSO 4(K) Ca +2 (s) + SO 4-2 Ca +2 SO 4-2 CaSO 4(K) * Katısıyla dengede olan doymuştur. * Eklenen su dipteki katıyıda çözer. * İletkenlik değişmez. * Çözünürlük değişmez. * Kçç değişmez * Ca +2 SO -2 4 mol sayısı artar. * Buhar basıncı değişmez. ÖRNEK: CaCl 2 katısıyla dengedeki sulu çözeltisine sabit sıcaklıkta ; 1- CaCl 2 katısı 2- NaCl katısı 3- Katının bir kısmını çözecek kadar saf su eklenmesi İşlemleri ayrı ayrı uygulanıyor. Buna göre hangilerinde Ca +2 derişimi azalır? 9
10 ÖRNEK: Suda az çözünen PbCl 2 tuzunun katısı ile dengedeki çözeltisine ayrı ayrı uygulanan; 1- Çözeltiyi ısıtma 2- Aynı sıcaklıkta su ekleme 3- Aynı sıcaklıkta PbCl 2 katısı ekleme İşlemlerinin hangilerinde Pb +2 iyonu mol sayısının artacağı kesindir? ÖRNEK: XY 2(K) XY 2(S) H 0 doygun çözeltisinde çözünürlüğü artırmak için; 1- Su eklemek 2- XY 2(K) eklemek 3- Sıcaklığı artırmak İşlemlerinden hangileri ayrı ayrı yapılmalıdır? 10
11 11
Fiziksel özellikleri her yerde aynı olan (homojen) karışımlara çözelti denir. Bir çözeltiyi oluşturan her bir maddeye çözeltinin bileşenleri denir.
 GENEL KİMYA 1 LABORATUARI ÇALIŞMA NOTLARI DENEY: 8 ÇÖZELTİLER Dr. Bahadır KESKİN, 2011 @ YTÜ Fiziksel özellikleri her yerde aynı olan (homojen) karışımlara çözelti denir. Bir çözeltiyi oluşturan her bir
GENEL KİMYA 1 LABORATUARI ÇALIŞMA NOTLARI DENEY: 8 ÇÖZELTİLER Dr. Bahadır KESKİN, 2011 @ YTÜ Fiziksel özellikleri her yerde aynı olan (homojen) karışımlara çözelti denir. Bir çözeltiyi oluşturan her bir
Çözünürlük kuralları
 Çözünürlük kuralları Bütün amonyum, bileşikleri suda çok çözünürler. Alkali metal (Grup IA) bileşikleri suda çok çözünürler. Klorür (Cl ), bromür (Br ) ve iyodür (I ) bileşikleri suda çok çözünürler, ancak
Çözünürlük kuralları Bütün amonyum, bileşikleri suda çok çözünürler. Alkali metal (Grup IA) bileşikleri suda çok çözünürler. Klorür (Cl ), bromür (Br ) ve iyodür (I ) bileşikleri suda çok çözünürler, ancak
5. ÇÖZÜNÜRLÜK DENGESİ
 5. ÇÖZÜNÜRLÜK DENGESİ Birçok tuz suda çok az çözünür. Tuzların sudaki çözünürlüğünden faydalanarak çökelek oluşumu kontrol edilebilir ve çökme olayı karışımları ayırmak için kullanılabilir. Çözünürlük
5. ÇÖZÜNÜRLÜK DENGESİ Birçok tuz suda çok az çözünür. Tuzların sudaki çözünürlüğünden faydalanarak çökelek oluşumu kontrol edilebilir ve çökme olayı karışımları ayırmak için kullanılabilir. Çözünürlük
ÇÖZÜNÜRLÜK ÇÖZÜNÜRLÜĞE ETKİ EDEN FAKTÖRLER
 ÇÖZÜNÜRLÜK ÇÖZÜNÜRLÜĞE ETKİ EDEN FAKTÖRLER ÇÖZÜNÜRLÜK Belirli sıcaklık ve basınçta genelde 100 g suda çözünen maksimum madde miktarına çözünürlük denir. Çözünürlük t C de X gr / 100 gr su olarak ifade
ÇÖZÜNÜRLÜK ÇÖZÜNÜRLÜĞE ETKİ EDEN FAKTÖRLER ÇÖZÜNÜRLÜK Belirli sıcaklık ve basınçta genelde 100 g suda çözünen maksimum madde miktarına çözünürlük denir. Çözünürlük t C de X gr / 100 gr su olarak ifade
4. ÇÖZÜNÜRLÜK. Çözünürlük Çarpımı Kçç. NaCl Na+ + Cl- (%100 iyonlaşma) AgCl(k) Ag + (ç) + Cl - (ç) (Kimyasal dengeye göre iyonlaşma) K = [AgCl(k)]
![4. ÇÖZÜNÜRLÜK. Çözünürlük Çarpımı Kçç. NaCl Na+ + Cl- (%100 iyonlaşma) AgCl(k) Ag + (ç) + Cl - (ç) (Kimyasal dengeye göre iyonlaşma) K = [AgCl(k)] 4. ÇÖZÜNÜRLÜK. Çözünürlük Çarpımı Kçç. NaCl Na+ + Cl- (%100 iyonlaşma) AgCl(k) Ag + (ç) + Cl - (ç) (Kimyasal dengeye göre iyonlaşma) K = [AgCl(k)]](/thumbs/69/61024076.jpg) 4. ÇÖZÜNÜRLÜK Çözünürlük Çarpımı NaCl Na+ + Cl- (%100 iyonlaşma) AgCl(k) Ag + (ç) + Cl - (ç) (Kimyasal dengeye göre iyonlaşma) + - [Ag ][Cl ] K = [AgCl(k)] K [AgCl(k)] = [Ag + ] [Cl - ] = [Ag + ] [Cl -
4. ÇÖZÜNÜRLÜK Çözünürlük Çarpımı NaCl Na+ + Cl- (%100 iyonlaşma) AgCl(k) Ag + (ç) + Cl - (ç) (Kimyasal dengeye göre iyonlaşma) + - [Ag ][Cl ] K = [AgCl(k)] K [AgCl(k)] = [Ag + ] [Cl - ] = [Ag + ] [Cl -
ÇÖZÜNÜRLÜK DENGESİ (Kçç)
 ÇÖZÜNÜRLÜK DENGESİ (Kçç) ÇÖZELTİLERDE ÇÖZÜNME VE ÇÖKELME OLAYLARI Çözeltiler doymuşluklarına göre üçe ayrılırlar: 1- Doymamış çözeltiler: Belirli bir sıcaklıkta ve basınçta çözebileceğinden daha az miktarda
ÇÖZÜNÜRLÜK DENGESİ (Kçç) ÇÖZELTİLERDE ÇÖZÜNME VE ÇÖKELME OLAYLARI Çözeltiler doymuşluklarına göre üçe ayrılırlar: 1- Doymamış çözeltiler: Belirli bir sıcaklıkta ve basınçta çözebileceğinden daha az miktarda
Sulu Çözeltiler ve Kimyasal Denge
 Sulu Çözeltiler ve Kimyasal Denge Sulu Çözeltiler Çözelti: iki veya daha fazla maddenin meydana getirdiği homojen karışımdır. çözücü, Kütlece fazla olan (veya çözme işlemini yapan) bileşene çözücü denir.
Sulu Çözeltiler ve Kimyasal Denge Sulu Çözeltiler Çözelti: iki veya daha fazla maddenin meydana getirdiği homojen karışımdır. çözücü, Kütlece fazla olan (veya çözme işlemini yapan) bileşene çözücü denir.
TURUNCU RENGĐN DANSI NASIL OLUR?
 KĐMYA EĞĐE ĞĐTĐM M SEMĐNER NERĐ PROF. DR. ĐNCĐ MORGĐL TURUNCU RENGĐN DANSI NASIL OLUR? HAZIRLAYAN: GÜLÇĐN YALLI KONU: ÇÖZELTĐLER KONU BAŞLIĞI: TURUNCU RENGĐN DANSI NASIL OLUR? ÇÖZELTĐLER Fiziksel özellikleri
KĐMYA EĞĐE ĞĐTĐM M SEMĐNER NERĐ PROF. DR. ĐNCĐ MORGĐL TURUNCU RENGĐN DANSI NASIL OLUR? HAZIRLAYAN: GÜLÇĐN YALLI KONU: ÇÖZELTĐLER KONU BAŞLIĞI: TURUNCU RENGĐN DANSI NASIL OLUR? ÇÖZELTĐLER Fiziksel özellikleri
Kompleks İyon Dengeleri
 ÜNİTE 10 Çözünürlük ve Kompleks İyon Dengeleri Amaçlar Bu üniteyi çalıştıktan sonra; Çözünürlük çarpımı sabiti kavramını öğrenecek, Çözünürlük ve Kçç arasındaki ilişkiyi kullanarak çözünürlük problemlerini
ÜNİTE 10 Çözünürlük ve Kompleks İyon Dengeleri Amaçlar Bu üniteyi çalıştıktan sonra; Çözünürlük çarpımı sabiti kavramını öğrenecek, Çözünürlük ve Kçç arasındaki ilişkiyi kullanarak çözünürlük problemlerini
00213 ANALİTİK KİMYA-I SINAV VE ÇALIŞMA SORULARI
 00213 ANALİTİK KİMYA-I SINAV VE ÇALIŞMA SORULARI A) TANIMLAR, KAVRAMLAR ve TEMEL HESAPLAMALAR: 1. Aşağıdaki kavramları birer cümle ile tanımlayınız. Analitik kimya, Sistematik analiz, ph, Tesir değerliği,
00213 ANALİTİK KİMYA-I SINAV VE ÇALIŞMA SORULARI A) TANIMLAR, KAVRAMLAR ve TEMEL HESAPLAMALAR: 1. Aşağıdaki kavramları birer cümle ile tanımlayınız. Analitik kimya, Sistematik analiz, ph, Tesir değerliği,
İnstagram:kimyaci_glcn_hoca H A 9.HAMLE SULU ÇÖZELTİLERDE DENGE ASİT VE BAZ DENGESİ 2.BÖLÜM. kimyaci_glcn_hoca
 13 H A M L E D E 9.HAMLE SULU ÇÖZELTİLERDE DENGE ASİT VE BAZ DENGESİ 2.BÖLÜM ZAYIF ASİT VE ZAYIF BAZ İYONLAŞMA YÜZDESİ 0,1 M Kuvvetli Asit HBr 1. Her iki asit çözeltisinin hacimleri ve derişimleri eşit
13 H A M L E D E 9.HAMLE SULU ÇÖZELTİLERDE DENGE ASİT VE BAZ DENGESİ 2.BÖLÜM ZAYIF ASİT VE ZAYIF BAZ İYONLAŞMA YÜZDESİ 0,1 M Kuvvetli Asit HBr 1. Her iki asit çözeltisinin hacimleri ve derişimleri eşit
4. Açısal momentum kuantum sayısı (,) 2 olan bir orbital türü ile ilgili, 5. Orbitaller Maksimum elektron sayısı
 Kuantum Sayıları Ve rbitaller 1. Başkuantum sayısı (n) belirtilen temel enerji düzeylerinden hangisinde bulunabilecek maksimum orbital sayısı yanlış verilmiştir? Başkuantum sayısı (n) Maksimum orbital
Kuantum Sayıları Ve rbitaller 1. Başkuantum sayısı (n) belirtilen temel enerji düzeylerinden hangisinde bulunabilecek maksimum orbital sayısı yanlış verilmiştir? Başkuantum sayısı (n) Maksimum orbital
ÇÖZÜNÜRLÜK (ORTAK İYON ETKİSİ ) (Çöktürme ile Ayırma)
 ÇÖZÜNÜRLÜ (ORTA İYON ETİSİ ) (Çöktürme ile Ayırma) Prof. Dr. ustafa DEİR 08ORTA İYON ETİSİ07B ÇÖZÜNÜRLÜ ÇÖTÜRE İLE AYIRA 1 ORTA İYON ETİSİ 08ORTA İYON ETİSİ07B ÇÖZÜNÜRLÜ ÇÖTÜRE İLE AYIRA ORTA İYON ETİSİ
ÇÖZÜNÜRLÜ (ORTA İYON ETİSİ ) (Çöktürme ile Ayırma) Prof. Dr. ustafa DEİR 08ORTA İYON ETİSİ07B ÇÖZÜNÜRLÜ ÇÖTÜRE İLE AYIRA 1 ORTA İYON ETİSİ 08ORTA İYON ETİSİ07B ÇÖZÜNÜRLÜ ÇÖTÜRE İLE AYIRA ORTA İYON ETİSİ
KĐMYA EĞĐTĐMĐ DERSĐ PROF.DR.ĐNCĐ MORGĐL
 KĐMYA EĞĐE ĞĐTĐMĐ DERSĐ PROF.DR.ĐNC NCĐ MORGĐL SINIF:11 DERS SAATĐ:4 KĐMYASAL REAKSĐYONLAR Sulu çözeltilerde olan reaksiyonlar Sulu çözeltilerde çökelme ve çözünme ile ilgili kurallar Gaz çıkışıışı olan
KĐMYA EĞĐE ĞĐTĐMĐ DERSĐ PROF.DR.ĐNC NCĐ MORGĐL SINIF:11 DERS SAATĐ:4 KĐMYASAL REAKSĐYONLAR Sulu çözeltilerde olan reaksiyonlar Sulu çözeltilerde çökelme ve çözünme ile ilgili kurallar Gaz çıkışıışı olan
T.C. Ölçme, Seçme ve Yerleştirme Merkezi
 T.C. Ölçme, Seçme ve Yerleştirme Merkezi LİSANS YERLEŞTİRME SINAVI-2 KİMYA TESTİ 17 HAZİRAN 2017 CUMARTESİ Bu testlerin her hakkı saklıdır. Hangi amaçla olursa olsun, testlerin tamamının veya bir kısmının
T.C. Ölçme, Seçme ve Yerleştirme Merkezi LİSANS YERLEŞTİRME SINAVI-2 KİMYA TESTİ 17 HAZİRAN 2017 CUMARTESİ Bu testlerin her hakkı saklıdır. Hangi amaçla olursa olsun, testlerin tamamının veya bir kısmının
ÇÖZELTİLERİN KOLİGATİF ÖZELLİKLERİ
 ÇÖZELTİLERİN KOLİGATİF ÖZELLİKLERİ Çözeltilerin sadece derişimine bağlı olarak değişen özelliklerine koligatif özellikler denir. Buhar basıncı düşmesi, Kaynama noktası yükselmesi, Donma noktası azalması
ÇÖZELTİLERİN KOLİGATİF ÖZELLİKLERİ Çözeltilerin sadece derişimine bağlı olarak değişen özelliklerine koligatif özellikler denir. Buhar basıncı düşmesi, Kaynama noktası yükselmesi, Donma noktası azalması
İnstagram:kimyaci_glcn_hoca SIVI ÇÖZELTİLER VE ÇÖZÜNÜRLÜK. kimyaci_glcn_hoca
 SIVI ÇÖZELTİLER VE ÇÖZÜNÜRLÜK SIVI ÇÖZELTİLER H 2 O, CH 3 CI, HF, H 2 S gibi moleküller; *Sıvılar ise polardır. * Bu tür maddeler dipol dipol etkileşimi oluşturur *Birbiri içerisinde *Çözelti:Çözünen +
SIVI ÇÖZELTİLER VE ÇÖZÜNÜRLÜK SIVI ÇÖZELTİLER H 2 O, CH 3 CI, HF, H 2 S gibi moleküller; *Sıvılar ise polardır. * Bu tür maddeler dipol dipol etkileşimi oluşturur *Birbiri içerisinde *Çözelti:Çözünen +
Kimya Mühendisliği Bölümü, 2014/2015 Öğretim Yılı, Bahar Yarıyılı 0102-Genel Kimya-II Dersi, Dönem Sonu Sınavı
 Kimya Mühendisliği Bölümü, 2014/2015 Öğretim Yılı, Bahar Yarıyılı 0102-Genel Kimya-II Dersi, Dönem Sonu Sınavı 20.05.2015 Soru (puan) 1 (20 ) 2 (20 ) 3 (20 ) 4 (25) 5 (20 ) 6 (20 ) Toplam Alınan Puan Not:
Kimya Mühendisliği Bölümü, 2014/2015 Öğretim Yılı, Bahar Yarıyılı 0102-Genel Kimya-II Dersi, Dönem Sonu Sınavı 20.05.2015 Soru (puan) 1 (20 ) 2 (20 ) 3 (20 ) 4 (25) 5 (20 ) 6 (20 ) Toplam Alınan Puan Not:
5) Çözünürlük(Xg/100gsu)
 1) I. Havanın sıvılaştırılması II. abrika bacasından çıkan SO 3 gazının H 2 O ile birleşmesi III. Na metalinin suda çözünmesi Yukardaki olaylardan hangilerinde kimyasal değişme gerçekleşir? 4) Kütle 1
1) I. Havanın sıvılaştırılması II. abrika bacasından çıkan SO 3 gazının H 2 O ile birleşmesi III. Na metalinin suda çözünmesi Yukardaki olaylardan hangilerinde kimyasal değişme gerçekleşir? 4) Kütle 1
II. Bileşenlerinin özelliklerini taşırlar. III. Hacimleri, çözücü ve çözünen hacimleri toplamına eşittir. yargılarından hangileri doğrudur?
 Sıvı Çözeltiler / Çözünme ve Derişim / Sıvı Ortamda Çözünme Olayı BÖLÜM 4 Test. Çözeltiler ile ilgili, I. Homojen karışımlardır. II. Bileşenlerinin özelliklerini taşırlar. III. Hacimleri, çözücü ve çözünen
Sıvı Çözeltiler / Çözünme ve Derişim / Sıvı Ortamda Çözünme Olayı BÖLÜM 4 Test. Çözeltiler ile ilgili, I. Homojen karışımlardır. II. Bileşenlerinin özelliklerini taşırlar. III. Hacimleri, çözücü ve çözünen
KİMYASAL REAKSİYONLARDA DENGE
 KİMYASAL REAKSİYONLARDA DENGE KİMYASAL REAKSİYONLARDA DENGE Kimyasal reaksiyonlar koşullar uygun olduğunda hem ileri hem de geri yönde gerçekleşirler. Böyle tepkimelere tersinir ya da denge tepkimeleri
KİMYASAL REAKSİYONLARDA DENGE KİMYASAL REAKSİYONLARDA DENGE Kimyasal reaksiyonlar koşullar uygun olduğunda hem ileri hem de geri yönde gerçekleşirler. Böyle tepkimelere tersinir ya da denge tepkimeleri
Kimyafull Gülçin Hoca
 KOLLİGATİF ÖZELLİKLER Kimyafull Gülçin Hoca Buhar basıncının düşmesi Kaynama sıcaklığının yükselmesi Donma sıcaklığının düşmesi Ozmotik basınç A) BUHAR BASINCI DÜŞMESİ RAOULT yasası: Bir çözeltiyi oluşturan
KOLLİGATİF ÖZELLİKLER Kimyafull Gülçin Hoca Buhar basıncının düşmesi Kaynama sıcaklığının yükselmesi Donma sıcaklığının düşmesi Ozmotik basınç A) BUHAR BASINCI DÜŞMESİ RAOULT yasası: Bir çözeltiyi oluşturan
Genel Kimya. Bölüm 7: ÇÖZELTİLER VE ÇÖZÜNÜRLÜK. Yrd. Doç. Dr. Mustafa SERTÇELİK Kafkas Üniversitesi Kimya Mühendisliği Bölümü
 Genel Kimya Bölüm 7: ÇÖZELTİLER VE ÇÖZÜNÜRLÜK Yrd. Doç. Dr. Mustafa SERTÇELİK Kafkas Üniversitesi Kimya Mühendisliği Bölümü ÇÖZELTİ VE TÜRLERİ Eğer bir madde diğer bir madde içinde molekül, atom veya iyonları
Genel Kimya Bölüm 7: ÇÖZELTİLER VE ÇÖZÜNÜRLÜK Yrd. Doç. Dr. Mustafa SERTÇELİK Kafkas Üniversitesi Kimya Mühendisliği Bölümü ÇÖZELTİ VE TÜRLERİ Eğer bir madde diğer bir madde içinde molekül, atom veya iyonları
YouTube:Kimyafull Gülçin Hoca Serüveni DERİŞİM BİRİMLERİ Ppm-ppb SORU ÇÖZÜMLERİ
 Serüveni DERİŞİM BİRİMLERİ Ppm-ppb SORU ÇÖZÜMLERİ ppm Toplam madde miktarının milyonda 1 birimlik maddesine denir. NOT: 1 kg su = 1 Litre ppm =. 10 6 1 kg çözeltide çözünen maddenin mg olarak kütlesine
Serüveni DERİŞİM BİRİMLERİ Ppm-ppb SORU ÇÖZÜMLERİ ppm Toplam madde miktarının milyonda 1 birimlik maddesine denir. NOT: 1 kg su = 1 Litre ppm =. 10 6 1 kg çözeltide çözünen maddenin mg olarak kütlesine
Bu tepkimelerde, iki ya da daha fazla element birleşmesi ile yeni bir bileşik oluşur. A + B AB CO2 + H2O H2CO3
 DENEY 2 BİLEŞİKLERİN TEPKİMELERİ İLE TANINMASI 2.1. AMAÇ Bileşiklerin verdiği tepkimelerin incelenmesi ve bileşiklerin tanınmasında kullanılması 2.2. TEORİ Kimyasal tepkime bir ya da daha fazla saf maddenin
DENEY 2 BİLEŞİKLERİN TEPKİMELERİ İLE TANINMASI 2.1. AMAÇ Bileşiklerin verdiği tepkimelerin incelenmesi ve bileşiklerin tanınmasında kullanılması 2.2. TEORİ Kimyasal tepkime bir ya da daha fazla saf maddenin
DENGEYE ETKİ EDEN FAKTÖRLER
 DENGEYE ETKİ EDEN FAKTÖRLER Le Chatelier(Lö Şatölye İlkesi) Bu ilkeye göre ; denge halinde bulunan sisteme dışarıdan bir etki yapıldığında sistem kendiliğinden bu etkiyi azaltacak yönde eğilim gösterir.
DENGEYE ETKİ EDEN FAKTÖRLER Le Chatelier(Lö Şatölye İlkesi) Bu ilkeye göre ; denge halinde bulunan sisteme dışarıdan bir etki yapıldığında sistem kendiliğinden bu etkiyi azaltacak yönde eğilim gösterir.
KİMYA II DERS NOTLARI
 KİMYA II DERS NOTLARI Yrd. Doç. Dr. Atilla EVCİN Sulu Çözeltilerin Doğası Elektrolitler Metallerde elektronların hareketiyle elektrik yükü taşınır. Saf su Suda çözünmüş Oksijen gazı Çözeltideki moleküllerin
KİMYA II DERS NOTLARI Yrd. Doç. Dr. Atilla EVCİN Sulu Çözeltilerin Doğası Elektrolitler Metallerde elektronların hareketiyle elektrik yükü taşınır. Saf su Suda çözünmüş Oksijen gazı Çözeltideki moleküllerin
ASİT-BAZ DENGESİ ÖSS DE ÇIKMIŞ SORULAR
 1. Amonyağın, NH 3, baz özelliği gösterdiğini açıklayan denklem aşağıdakilerden hangisidir? A) NH 3(gaz) NH 3(sıvı) B) N 2(gaz) + 3H 2(gaz) 2NH 3(gaz) C) 2NH 3(gaz) +5/2O 2(gaz) 2NO (gaz) + 3H 2 O (gaz)
1. Amonyağın, NH 3, baz özelliği gösterdiğini açıklayan denklem aşağıdakilerden hangisidir? A) NH 3(gaz) NH 3(sıvı) B) N 2(gaz) + 3H 2(gaz) 2NH 3(gaz) C) 2NH 3(gaz) +5/2O 2(gaz) 2NO (gaz) + 3H 2 O (gaz)
4. Oksijen bileşiklerinde 2, 1, 1/2 veya +2 değerliklerini (N Metil: CH 3. Cevap C. Adı. 6. X bileşiği C x. Cevap E. n O2. C x.
 ÇÖZÜMLER. E foton h υ 6.0 34. 0 7 6.0 7 Joule Elektronun enerjisi E.0 8 n. (Z).0 8 (). () 8.0 8 Joule 0,8.0 7 Joule 4. ksijen bileşiklerinde,, / veya + değerliklerini alabilir. Klorat iyonu Cl 3 dir. (N
ÇÖZÜMLER. E foton h υ 6.0 34. 0 7 6.0 7 Joule Elektronun enerjisi E.0 8 n. (Z).0 8 (). () 8.0 8 Joule 0,8.0 7 Joule 4. ksijen bileşiklerinde,, / veya + değerliklerini alabilir. Klorat iyonu Cl 3 dir. (N
A A A A A A A A A A A
 LYS 2 KİMYA TESTİ 1. Bu testte 30 soru vardır. 2. Cevaplarınızı, cevap kâğıdının Kimya Testi için ayrılan kısmına işaretleyiniz. 1. Eşit miktarlardaki suda; 3.. 36 gram Fe(NO 3 ) 2. n mol NaCl çözülerek
LYS 2 KİMYA TESTİ 1. Bu testte 30 soru vardır. 2. Cevaplarınızı, cevap kâğıdının Kimya Testi için ayrılan kısmına işaretleyiniz. 1. Eşit miktarlardaki suda; 3.. 36 gram Fe(NO 3 ) 2. n mol NaCl çözülerek
7-2. Aşağıdakileri kısaca tanımlayınız veya açıklayınız. a) Amfiprotik çözücü b) Farklandırıcı çözücü c) Seviyeleme çözücüsü d) Kütle etkisi
 SKOOG 7-1. Aşağıdakileri kısaca tanımlayınız veya açıklayınız. a) Zayıf elektrolit b) Bronsted-Lowry asidi c) Bronsted-Lowry asidinin konjuge bazı d) Bronsted-Lowry tanımına dayanarak nötralleşme e) Amfiprotik
SKOOG 7-1. Aşağıdakileri kısaca tanımlayınız veya açıklayınız. a) Zayıf elektrolit b) Bronsted-Lowry asidi c) Bronsted-Lowry asidinin konjuge bazı d) Bronsted-Lowry tanımına dayanarak nötralleşme e) Amfiprotik
6.PPB (milyarda bir kısım) Kaynakça Tablo A-1: Çözelti Örnekleri... 5 Tablo B-1:Kolloidal Tanecikler... 8
 İçindekiler A. ÇÖZELTİLER... 2 1.Çözünme... 2 2.Homojenlik... 4 3.Çözelti... 5 4.Çözünürlük... 5 Çözünürlüğe Sıcaklık Ve Basınç Etkisi... 6 B. KARIŞIMLAR... 7 1.Çözeltiler... 7 2.Kolloidal Karışımlar...
İçindekiler A. ÇÖZELTİLER... 2 1.Çözünme... 2 2.Homojenlik... 4 3.Çözelti... 5 4.Çözünürlük... 5 Çözünürlüğe Sıcaklık Ve Basınç Etkisi... 6 B. KARIŞIMLAR... 7 1.Çözeltiler... 7 2.Kolloidal Karışımlar...
GENEL KİMYA. Yrd.Doç.Dr. Tuba YETİM
 GENEL KİMYA ÇÖZELTİLER Homojen karışımlara çözelti denir. Çözelti bileşiminin ve özelliklerinin çözeltinin her yerinde aynı olması sebebiyle çözelti, «homojen» olarak nitelendirilir. Çözeltinin değişen
GENEL KİMYA ÇÖZELTİLER Homojen karışımlara çözelti denir. Çözelti bileşiminin ve özelliklerinin çözeltinin her yerinde aynı olması sebebiyle çözelti, «homojen» olarak nitelendirilir. Çözeltinin değişen
KİMYASAL TEPKİMELERDE DENGE II
 KİMYASAL TEPKİMELERDE DENGE II Kimyasal tepkimelerde denge, sıcaklık, basınç ve denge bağıntısında yer alan maddelerin derişimlerine bağlıdır. Denge halindeki bir sistemde bu üç etkenden birini değiştirerek,
KİMYASAL TEPKİMELERDE DENGE II Kimyasal tepkimelerde denge, sıcaklık, basınç ve denge bağıntısında yer alan maddelerin derişimlerine bağlıdır. Denge halindeki bir sistemde bu üç etkenden birini değiştirerek,
Doğal Rb elementinin atom kütlesi 85,47 g/mol dür ve atom kütleleri 84,91 g/mol olan 86 Rb ile 86,92 olan 87
 Doğal Rb elementinin atom kütlesi 85,47 g/mol dür ve atom kütleleri 84,91 g/mol olan 86 Rb ile 86,92 olan 87 Rb izotoplarından oluşmuştur. İzotopların doğada bulunma yüzdelerini hesaplayınız. Bir bileşik
Doğal Rb elementinin atom kütlesi 85,47 g/mol dür ve atom kütleleri 84,91 g/mol olan 86 Rb ile 86,92 olan 87 Rb izotoplarından oluşmuştur. İzotopların doğada bulunma yüzdelerini hesaplayınız. Bir bileşik
HEDEF VE DAVRANIŞLAR:
 HEDEF VE DAVRANIŞLAR: 1) Çözünürlük konusuna giriş yapılır ve günlük hayattan örnekler vererek anlaşılmasının sağlanır. 2) Çözünürlüğe etki eden faktörlerin anlatılır ve örneklerle pekiştirilir. 3) Çözünürlüğe
HEDEF VE DAVRANIŞLAR: 1) Çözünürlük konusuna giriş yapılır ve günlük hayattan örnekler vererek anlaşılmasının sağlanır. 2) Çözünürlüğe etki eden faktörlerin anlatılır ve örneklerle pekiştirilir. 3) Çözünürlüğe
Çözeltiler. MÜHENDİSLİK KİMYASI DERS NOTLARI Yrd. Doç. Dr. Atilla EVCİN. Yrd. Doç. Dr. Atilla EVCİN Afyonkarahisar Kocatepe Üniversitesi 2006
 Çözeltiler Çözelti, iki veya daha fazla maddenin homojen bir karışımı olup, en az iki bileşenden oluşur. Bileşenlerden biri çözücü, diğeri ise çözünendir. MÜHENDİSLİK KİMYASI DERS NOTLARI Yrd. Doç. Dr.
Çözeltiler Çözelti, iki veya daha fazla maddenin homojen bir karışımı olup, en az iki bileşenden oluşur. Bileşenlerden biri çözücü, diğeri ise çözünendir. MÜHENDİSLİK KİMYASI DERS NOTLARI Yrd. Doç. Dr.
Çözünürlük ve Çözünürlüğe Etki Eden Faktörler
 Çözünürlük ve Çözünürlüğe Etki Eden Faktörler Yazar Yrd. Doç. Dr. Nevin KANIŞKAN ÜNİTE 12 Amaçlar Bu üniteyi çalıştıktan sonra; çözünürlük çarpımı kavramını öğrenecek, molar çözünürlük ve çözünürlük kavramlarını
Çözünürlük ve Çözünürlüğe Etki Eden Faktörler Yazar Yrd. Doç. Dr. Nevin KANIŞKAN ÜNİTE 12 Amaçlar Bu üniteyi çalıştıktan sonra; çözünürlük çarpımı kavramını öğrenecek, molar çözünürlük ve çözünürlük kavramlarını
ÜN TE III ÇÖZÜNÜRLÜK DENGELER
 ÜN TE III ÇÖZÜNÜRLÜK DENGELER 3. 1. ÇÖZÜNME OLAYI 3. 2. SIVI-KATI ÇÖZELT LER 3. 3. SIVI-SIVI ÇÖZELT LER 3. 4. SIVI-GAZ ÇÖZELT LER 3. 5. ÇÖZÜNME OLAYINDA DÜZENS ZL K FAKTÖRÜ 3. 6. SULU ÇÖZELT LER a) Elektrolit
ÜN TE III ÇÖZÜNÜRLÜK DENGELER 3. 1. ÇÖZÜNME OLAYI 3. 2. SIVI-KATI ÇÖZELT LER 3. 3. SIVI-SIVI ÇÖZELT LER 3. 4. SIVI-GAZ ÇÖZELT LER 3. 5. ÇÖZÜNME OLAYINDA DÜZENS ZL K FAKTÖRÜ 3. 6. SULU ÇÖZELT LER a) Elektrolit
Serüveni 3.ÜNİTE:KİMYASAL TÜRLER ARASI ETKİLEŞİM FİZİKSEL VE KİMYASAL DEĞİŞİM KİMYASAL TEPKİME TÜRLERİ
 Serüveni 3.ÜNİTE:KİMYASAL TÜRLER ARASI ETKİLEŞİM FİZİKSEL VE KİMYASAL DEĞİŞİM KİMYASAL TEPKİME TÜRLERİ FİZİKSEL VE KİMYASAL DEĞİŞİM FİZİKSEL DEĞİŞİM Beş duyu organımızla algıladığımız fiziksel özelliklerdeki
Serüveni 3.ÜNİTE:KİMYASAL TÜRLER ARASI ETKİLEŞİM FİZİKSEL VE KİMYASAL DEĞİŞİM KİMYASAL TEPKİME TÜRLERİ FİZİKSEL VE KİMYASAL DEĞİŞİM FİZİKSEL DEĞİŞİM Beş duyu organımızla algıladığımız fiziksel özelliklerdeki
a. Yükseltgenme potansiyeli büyük olanlar daha aktifdir.
 ELEKTROKİMYA A. AKTİFLİK B. PİLLER C. ELEKTROLİZ A. AKTİFLİK Metallerin elektron verme, ametallerin elektron alma yatkınlıklarına aktiflik denir. Yani bir metal ne kadar kolay elektron veriyorsa bir ametal
ELEKTROKİMYA A. AKTİFLİK B. PİLLER C. ELEKTROLİZ A. AKTİFLİK Metallerin elektron verme, ametallerin elektron alma yatkınlıklarına aktiflik denir. Yani bir metal ne kadar kolay elektron veriyorsa bir ametal
SULU ÇÖZELTİLERDE DENGE
 İMYASAL DENGE SULU ÇÖZELTİLERDE DENGE Prof. Dr. Mustafa DEMİR M.DEMİR 06-İMYASAL DENGE 1 SULU ÇÖZELTİLERDE DENGE Bileşikler suda, özelliklerine göre az veya çok oranda ayrışarak iyonlaşırlar. İyon içeren
İMYASAL DENGE SULU ÇÖZELTİLERDE DENGE Prof. Dr. Mustafa DEMİR M.DEMİR 06-İMYASAL DENGE 1 SULU ÇÖZELTİLERDE DENGE Bileşikler suda, özelliklerine göre az veya çok oranda ayrışarak iyonlaşırlar. İyon içeren
KİMYASAL TEPKİMELERDE HIZ
 KİMYASAL TEPKİMELERDE IZ TEPKİME IZI Kimyasal bir tepkime sırasında, tepkimeye giren maddelerin miktarı giderek azalırken, ürünlerin miktarı giderek artar. Bir tepkimede, birim zamanda harcanan ya da oluşan
KİMYASAL TEPKİMELERDE IZ TEPKİME IZI Kimyasal bir tepkime sırasında, tepkimeye giren maddelerin miktarı giderek azalırken, ürünlerin miktarı giderek artar. Bir tepkimede, birim zamanda harcanan ya da oluşan
kimyasal değişimin sembol ve formüllerle ifade edilmesidir.
 myasal reaksiyon Bir (veya birden fazla ) madde nin etkileşim sonucu yeni madde(lere) dönüşmesi işlemidir. ziksel değişim - renk değişimi - çökelek oluşumu - gaz çıkışı - ısı değişimi imyasal denklem aktif
myasal reaksiyon Bir (veya birden fazla ) madde nin etkileşim sonucu yeni madde(lere) dönüşmesi işlemidir. ziksel değişim - renk değişimi - çökelek oluşumu - gaz çıkışı - ısı değişimi imyasal denklem aktif
LYS KİMYA DENEMESİ 1.SORU: 2.soru: I- 0,9 M Ca C sulu çözeltisi II- 0,6 M Ca ( N0 3 ) 2 sulu çözeltisi
 1.SRU: I- 0,9 M Ca C 2 0 4 sulu çözeltisi II- 0,6 M Ca ( N0 3 ) 2 sulu çözeltisi Yukarıda aynı koşullarda bulunan çözeltilerin aşağıdaki hangi nicelikleri eşit değildir? a)donmaya başlama sıcaklığı b)
1.SRU: I- 0,9 M Ca C 2 0 4 sulu çözeltisi II- 0,6 M Ca ( N0 3 ) 2 sulu çözeltisi Yukarıda aynı koşullarda bulunan çözeltilerin aşağıdaki hangi nicelikleri eşit değildir? a)donmaya başlama sıcaklığı b)
İLK ANYONLAR , PO 4. Cl -, SO 4 , CO 3 , NO 3
 İLK ANYONLAR Cl -, SO -, CO -, PO -, NO - İLK ANYONLAR Anyonlar negatif yüklü iyonlardır. Kalitatif analitik kimya analizlerine ilk anyonlar olarak adlandırılan Cl -, SO -, CO -, PO -, NO - analizi ile
İLK ANYONLAR Cl -, SO -, CO -, PO -, NO - İLK ANYONLAR Anyonlar negatif yüklü iyonlardır. Kalitatif analitik kimya analizlerine ilk anyonlar olarak adlandırılan Cl -, SO -, CO -, PO -, NO - analizi ile
Bir maddenin başka bir madde içerisinde homojen olarak dağılmasına ÇÖZÜNME denir. Çözelti=Çözücü+Çözünen
 ÇÖZÜCÜ VE ÇÖZÜNEN ETKİLEŞİMLERİ: Çözünme olayı ve Çözelti Oluşumu: Bir maddenin başka bir madde içerisinde homojen olarak dağılmasına ÇÖZÜNME denir. Çözelti=Çözücü+Çözünen Çözünme İyonik Çözünme Moleküler
ÇÖZÜCÜ VE ÇÖZÜNEN ETKİLEŞİMLERİ: Çözünme olayı ve Çözelti Oluşumu: Bir maddenin başka bir madde içerisinde homojen olarak dağılmasına ÇÖZÜNME denir. Çözelti=Çözücü+Çözünen Çözünme İyonik Çözünme Moleküler
M-DEMİR K213 Soru bankası ANALİTİK KİMYA I DERSİ SORULARI
 ANALİTİK KİMYA I DERSİ SORULARI 1. Örnek 1 : ph =4 tampon ortamında CaC2O4 çözünürlüğü nedir? Kcc= 1,7x10-9, Ka1= 5,6x10-2, Ka2= 5,42x10-5 2. Örnek 03: BaCO3 ın sudaki çözünürlüğü nedir?, Kçç=5.0x10-9,
ANALİTİK KİMYA I DERSİ SORULARI 1. Örnek 1 : ph =4 tampon ortamında CaC2O4 çözünürlüğü nedir? Kcc= 1,7x10-9, Ka1= 5,6x10-2, Ka2= 5,42x10-5 2. Örnek 03: BaCO3 ın sudaki çözünürlüğü nedir?, Kçç=5.0x10-9,
10-ÇÖKME VE ÇÖZÜNÜRLÜK ÇARPIMI
 ÇÖME VE ÇÖZÜNÜRLÜ Prof. Dr. Mustafa DEMİR M.DEMİR 10ÇÖME VE ÇÖZÜNÜRLÜ 1 M.DEMİR 10ÇÖME VE ÇÖZÜNÜRLÜ ÇÖZÜNÜRLÜ Çözeltilerle ilgili olarak verilen bilgiler genellikle tek fazlı homojen sistemleri kapsamaktadır.
ÇÖME VE ÇÖZÜNÜRLÜ Prof. Dr. Mustafa DEMİR M.DEMİR 10ÇÖME VE ÇÖZÜNÜRLÜ 1 M.DEMİR 10ÇÖME VE ÇÖZÜNÜRLÜ ÇÖZÜNÜRLÜ Çözeltilerle ilgili olarak verilen bilgiler genellikle tek fazlı homojen sistemleri kapsamaktadır.
Bölüm 5 Çalışma Soruları
 Bölüm 5 Çalışma Soruları 5.1) Metanol, CH 3 OH, ve hidrojen siyanür, HCN, bileşiklerinin her ikisi de moleküler bileşik olmasına rağmen metanol elektrik akımını iletmezken, hidrojen siyanür iletir. Neden?
Bölüm 5 Çalışma Soruları 5.1) Metanol, CH 3 OH, ve hidrojen siyanür, HCN, bileşiklerinin her ikisi de moleküler bileşik olmasına rağmen metanol elektrik akımını iletmezken, hidrojen siyanür iletir. Neden?
ASİTLER- BAZLAR. Suyun kendi kendine iyonlaşmasına Suyun Otonizasyonu - Otoprotoliz adı verilir. Suda oluşan H + sadece protondur.
 ASİTLER- BAZLAR SUYUN OTONİZASYONU: Suyun kendi kendine iyonlaşmasına Suyun Otonizasyonu - Otoprotoliz adı verilir. Suda oluşan H + sadece protondur. H 2 O (S) H + (suda) + OH - (Suda) H 2 O (S) + H +
ASİTLER- BAZLAR SUYUN OTONİZASYONU: Suyun kendi kendine iyonlaşmasına Suyun Otonizasyonu - Otoprotoliz adı verilir. Suda oluşan H + sadece protondur. H 2 O (S) H + (suda) + OH - (Suda) H 2 O (S) + H +
ÖN SÖZ. Üniversiteye hazırlık yolunda, yeni sınav sistemine uygun olarak hazırladığımız YKS Alan Yeterlilik
 ÖN SÖZ Sevgili Öğrenciler, Üniversiteye hazırlık yolunda, yeni sınav sistemine uygun olarak hazırladığımız YKS Alan Yeterlilik Testi Kimya Soru Bankası kitabımızı sizlere sunmaktan onur duyuyoruz. Başarınıza
ÖN SÖZ Sevgili Öğrenciler, Üniversiteye hazırlık yolunda, yeni sınav sistemine uygun olarak hazırladığımız YKS Alan Yeterlilik Testi Kimya Soru Bankası kitabımızı sizlere sunmaktan onur duyuyoruz. Başarınıza
... ANADOLU L SES 2009-2010 E T M YILI I. DÖNEM 11. SINIF K MYA DERS 1. YAZILI SINAVI SINIFI: Ö RENC NO: Ö RENC N N ADI VE SOYADI:
 ... ANADOLU L SES 2009-2010 E T M YILI I. DÖNEM 11. SINIF K MYA DERS 1. YAZILI SINAVI SINIFI: Ö RENC NO: Ö RENC N N ADI VE SOYADI: 1. Ca (k) + 2 H + (ag) Ca +2 (ag) + H 2(g) 5 litrelik bir kaba 0,1 mol
... ANADOLU L SES 2009-2010 E T M YILI I. DÖNEM 11. SINIF K MYA DERS 1. YAZILI SINAVI SINIFI: Ö RENC NO: Ö RENC N N ADI VE SOYADI: 1. Ca (k) + 2 H + (ag) Ca +2 (ag) + H 2(g) 5 litrelik bir kaba 0,1 mol
ÇÖZÜNME OLGUSU VE ÇÖZELTĐLER SÜRE : 2 DERS SAATĐ
 ÇÖZÜNME OLGUSU VE ÇÖZELTĐLER SÜRE : 2 DERS SAATĐ HAZIRLAYANLAR: NAZLI KIRCI ESRA N.ÇECE SUPHĐ SEVDĐ HEDEF VE DAVRANIŞLAR. HEDEF 1 : ÇÖZELTĐ VE ÖZELLĐKLERĐNĐ KAVRAYABĐLME DAVRANIŞLAR : 1. Çözünme kavramını
ÇÖZÜNME OLGUSU VE ÇÖZELTĐLER SÜRE : 2 DERS SAATĐ HAZIRLAYANLAR: NAZLI KIRCI ESRA N.ÇECE SUPHĐ SEVDĐ HEDEF VE DAVRANIŞLAR. HEDEF 1 : ÇÖZELTĐ VE ÖZELLĐKLERĐNĐ KAVRAYABĐLME DAVRANIŞLAR : 1. Çözünme kavramını
ELEKTROKİMYA II. www.kimyahocam.com
 ELEKTROKİMYA II ELEKTROKİMYASAL PİLLER Kendiliğinden gerçekleşen redoks tepkimelerinde elektron alışverişinden yararlanılarak, kimyasal bağ enerjisi elektrik enerjisine dönüştürülebilir. Kimyasal enerjiyi,
ELEKTROKİMYA II ELEKTROKİMYASAL PİLLER Kendiliğinden gerçekleşen redoks tepkimelerinde elektron alışverişinden yararlanılarak, kimyasal bağ enerjisi elektrik enerjisine dönüştürülebilir. Kimyasal enerjiyi,
HACETTEPE ÜNĐVERSĐTESĐ ÖĞRETĐM TEKNOLOJĐLERĐ VE MATERYAL GELĐŞTĐRME KONU ANLATIMI. Hazırlayan: Hale Sümerkan. Dersin Sorumlusu: Prof. Dr.
 HACETTEPE ÜNĐVERSĐTESĐ ÖĞRETĐM TEKNOLOJĐLERĐ VE MATERYAL GELĐŞTĐRME KONU ANLATIMI Hazırlayan: Hale Sümerkan Dersin Sorumlusu: Prof. Dr.Đnci Morgil ANKARA 2008 ÇÖZELTĐLER Çözeltiler, iki ya da daha fazla
HACETTEPE ÜNĐVERSĐTESĐ ÖĞRETĐM TEKNOLOJĐLERĐ VE MATERYAL GELĐŞTĐRME KONU ANLATIMI Hazırlayan: Hale Sümerkan Dersin Sorumlusu: Prof. Dr.Đnci Morgil ANKARA 2008 ÇÖZELTĐLER Çözeltiler, iki ya da daha fazla
 1. 250 ml 0,20 M CuSO 4 (aq) çözeltisi hazırlamak için gerekli olan CuSO 4.5H 2 O kütlesini bulunuz. Bu çözeltiden 100 ml 0,10 M CuSO 4 (aq) çözeltisini nasıl hazırlarsınız?( Cu: 63,5; S:32; O:16; H:1)
1. 250 ml 0,20 M CuSO 4 (aq) çözeltisi hazırlamak için gerekli olan CuSO 4.5H 2 O kütlesini bulunuz. Bu çözeltiden 100 ml 0,10 M CuSO 4 (aq) çözeltisini nasıl hazırlarsınız?( Cu: 63,5; S:32; O:16; H:1)
Üçüncü Tek Saatlik Sınav 5.111
 Sayfa 1 /10 Üçüncü Tek Saatlik Sınav 5.111 İsminizi aşağıya yazınız. Sınavda kitaplarınız kapalı olacaktır. 6 problemi de çözmelisiniz. Bir problemin bütün şıklarını baştan sona dikkatli bir şekilde okuyunuz.
Sayfa 1 /10 Üçüncü Tek Saatlik Sınav 5.111 İsminizi aşağıya yazınız. Sınavda kitaplarınız kapalı olacaktır. 6 problemi de çözmelisiniz. Bir problemin bütün şıklarını baştan sona dikkatli bir şekilde okuyunuz.
SULU DENGELERE KATILMA (İLAVE) DURUMLARI *BİR TAMPON ÇÖZELTİNİN NASIL FONKSİYON GÖSTERDİĞİNİ AÇIKLAMAK
 KONUNUN AMACI VE ANAHTAR KAVRAMLAR *ORTAK İYON ETKİSİNİ TANIMLAMAK SULU DENGELERE KATILMA (İLAVE) DURUMLARI *BİR TAMPON ÇÖZELTİNİN NASIL FONKSİYON GÖSTERDİĞİNİ AÇIKLAMAK *TAMPON ÇÖZELTİNİN PH INI HESAPLAMAK
KONUNUN AMACI VE ANAHTAR KAVRAMLAR *ORTAK İYON ETKİSİNİ TANIMLAMAK SULU DENGELERE KATILMA (İLAVE) DURUMLARI *BİR TAMPON ÇÖZELTİNİN NASIL FONKSİYON GÖSTERDİĞİNİ AÇIKLAMAK *TAMPON ÇÖZELTİNİN PH INI HESAPLAMAK
Sulu Çözeltilerde Asit - Baz Dengesi
 Bu notlara Youtube dan Kimya Elbistan kanalında ilgili videolarının açıklamalar kısmında ki linkten ücretsiz bir şekilde ulaşabilirsiniz. A. Asit ve Baz Tanımları Arrhenius Asit - Baz Tanımı Arrhenius
Bu notlara Youtube dan Kimya Elbistan kanalında ilgili videolarının açıklamalar kısmında ki linkten ücretsiz bir şekilde ulaşabilirsiniz. A. Asit ve Baz Tanımları Arrhenius Asit - Baz Tanımı Arrhenius
İnstagram:kimyaci_glcn_hoca H A 9.HAMLE SULU ÇÖZELTİLERDE DENGE ASİT VE BAZ DENGESİ. kimyaci_glcn_hoca
 13 H A M L E D E 9.HAMLE SULU ÇÖZELTİLERDE DENGE ASİT VE BAZ DENGESİ ASİTLER VE BAZLAR 1.Arrhenius Asit-Baz Tanımı Arrhenius a göre bir madde suda iyonlarına ayrışarak çözündüğünde ortamdaki; H + iyonları
13 H A M L E D E 9.HAMLE SULU ÇÖZELTİLERDE DENGE ASİT VE BAZ DENGESİ ASİTLER VE BAZLAR 1.Arrhenius Asit-Baz Tanımı Arrhenius a göre bir madde suda iyonlarına ayrışarak çözündüğünde ortamdaki; H + iyonları
11. SINIF KİMYA YAZ TATİLİ ÖDEV KİTAPÇIĞI
 11. SINIF KİMYA YAZ TATİLİ ÖDEV KİTAPÇIĞI Sevgili öğrenciler, oldukça yorucu ve yoğun 11.sınıf kimya programını başarıyla tamamlayarak tatili hak ettiniz. LYS de 30 tane kimya sorusunun 10 tanesi 11.sınıf
11. SINIF KİMYA YAZ TATİLİ ÖDEV KİTAPÇIĞI Sevgili öğrenciler, oldukça yorucu ve yoğun 11.sınıf kimya programını başarıyla tamamlayarak tatili hak ettiniz. LYS de 30 tane kimya sorusunun 10 tanesi 11.sınıf
KOLLİGATİF ÖZELLİKLER SORU ÇÖZÜMÜ
 KOLLİGATİF ÖZELLİKLER SORU ÇÖZÜMÜ KOLLİGATİF ÖZELLİKLER Çözeltinin derişimine bağlı özelliklerine KOLİGATİF ÖZELLİK denir. Kaynama noktası Buhar basıncı Donma noktası Osmotik Basınç Çözünen Madde çözündüğünde:
KOLLİGATİF ÖZELLİKLER SORU ÇÖZÜMÜ KOLLİGATİF ÖZELLİKLER Çözeltinin derişimine bağlı özelliklerine KOLİGATİF ÖZELLİK denir. Kaynama noktası Buhar basıncı Donma noktası Osmotik Basınç Çözünen Madde çözündüğünde:
Yrd. Doç. Dr. Atilla EVCİN Afyonkarahisar Kocatepe Üiversitesi 2007 KLERİ DERS NOTLARI. Sıvı fazdan katı taneciklerin çökelmesi için çoğu reaksiyonlar
 TOZ ÜRETİM TEKNİKLER KLERİ DERS NOTLARI YRD. DOÇ.. DR. ATİLLA EVCİN Kimyasal Çökeltme Sıvı fazdan katı taneciklerin çökelmesi için çoğu reaksiyonlar A + B AB tipi çökelme reaksiyonlarıdır. Kuvvetli atomlararası
TOZ ÜRETİM TEKNİKLER KLERİ DERS NOTLARI YRD. DOÇ.. DR. ATİLLA EVCİN Kimyasal Çökeltme Sıvı fazdan katı taneciklerin çökelmesi için çoğu reaksiyonlar A + B AB tipi çökelme reaksiyonlarıdır. Kuvvetli atomlararası
EYVAH ŞEKERĐM KAYBOLDU!!!!! 9. SINIF 4. ÜNĐTE KARIŞIMLAR
 EYVAH ŞEKERĐM KAYBOLDU!!!!! 9. SINIF 4. ÜNĐTE KARIŞIMLAR KĐMYA ĐLE ĐLĐŞKĐSĐ ve GÜNLÜK HAYATLA ĐLĐŞKĐSĐ ŞEKERĐN ÇAYDA YA DA BAŞKA BĐR SIVIDA KARIŞTIRILDIĞINDA KAYBOLMASI, KĐMYADA ÇÖZÜNME OLGUSUYLA AÇIKLANABĐLĐR.
EYVAH ŞEKERĐM KAYBOLDU!!!!! 9. SINIF 4. ÜNĐTE KARIŞIMLAR KĐMYA ĐLE ĐLĐŞKĐSĐ ve GÜNLÜK HAYATLA ĐLĐŞKĐSĐ ŞEKERĐN ÇAYDA YA DA BAŞKA BĐR SIVIDA KARIŞTIRILDIĞINDA KAYBOLMASI, KĐMYADA ÇÖZÜNME OLGUSUYLA AÇIKLANABĐLĐR.
ÇÖZÜNME ve ÇÖZÜNÜRLÜK
 ÇÖZÜNME ve ÇÖZÜNÜRLÜK Prof. Dr. Mustafa DEMİR M.DEMİR 05-ÇÖZÜNME VE ÇÖZÜNÜRLÜK 1 Çözünme Olayı Analitik kimyada çözücü olarak genellikle su kullanılır. Su molekülleri, bir oksijen atomuna bağlı iki hidrojen
ÇÖZÜNME ve ÇÖZÜNÜRLÜK Prof. Dr. Mustafa DEMİR M.DEMİR 05-ÇÖZÜNME VE ÇÖZÜNÜRLÜK 1 Çözünme Olayı Analitik kimyada çözücü olarak genellikle su kullanılır. Su molekülleri, bir oksijen atomuna bağlı iki hidrojen
AKTİVİTE VE KİMYASAL DENGE
 AKTİVİTE VE KİMYASAL DENGE (iyonik türlerin dengeye etkisi) Prof. Dr. Mustafa DEMİR M.DEMİR 11-AKTİVİTE VE KİMYASAL DENGE 1 Denge sabitinin tanımında tanecikler arası çekim kuvvetinin olmadığı (ideal çözelti)
AKTİVİTE VE KİMYASAL DENGE (iyonik türlerin dengeye etkisi) Prof. Dr. Mustafa DEMİR M.DEMİR 11-AKTİVİTE VE KİMYASAL DENGE 1 Denge sabitinin tanımında tanecikler arası çekim kuvvetinin olmadığı (ideal çözelti)
KİMYASAL DENGE. AMAÇ Bu deneyin amacı öğrencilerin reaksiyon denge sabitini,k, deneysel olarak bulmalarıdır.
 KİMYASAL DENGE AMAÇ Bu deneyin amacı öğrencilerin reaksiyon denge sabitini,k, deneysel olarak bulmalarıdır. TEORİ Bir kimyasal tepkimenin yönü bazı reaksiyonlar için tek bazıları için ise çift yönlüdür.
KİMYASAL DENGE AMAÇ Bu deneyin amacı öğrencilerin reaksiyon denge sabitini,k, deneysel olarak bulmalarıdır. TEORİ Bir kimyasal tepkimenin yönü bazı reaksiyonlar için tek bazıları için ise çift yönlüdür.
ÇÖZELTİLERDE DENGE (Asit-Baz)
 ÇÖZELTİLERDE DENGE (AsitBaz) SUYUN OTOİYONİZASYONU Saf suyun elektrik akımını iletmediği bilinir, ancak çok hassas ölçü aletleriyle yapılan deneyler sonucunda suyun çok zayıf da olsa iletken olduğu tespit
ÇÖZELTİLERDE DENGE (AsitBaz) SUYUN OTOİYONİZASYONU Saf suyun elektrik akımını iletmediği bilinir, ancak çok hassas ölçü aletleriyle yapılan deneyler sonucunda suyun çok zayıf da olsa iletken olduğu tespit
KARIŞIMLAR. Birden çok maddenin kimyasal bağ oluşturmadan bir arada bulunmasıyla meydana gelen mad-delere karışım denir.
 KARIŞIMLAR Birden çok maddenin kimyasal bağ oluşturmadan bir arada bulunmasıyla meydana gelen mad-delere karışım denir. 1-HETEROJEN KARIŞIMLAR (ADİ KARIŞIMLAR) Karışımı oluşturan maddeler karışımın her
KARIŞIMLAR Birden çok maddenin kimyasal bağ oluşturmadan bir arada bulunmasıyla meydana gelen mad-delere karışım denir. 1-HETEROJEN KARIŞIMLAR (ADİ KARIŞIMLAR) Karışımı oluşturan maddeler karışımın her
Aeresol. Süspansiyon. Heterojen Emülsiyon. Karışım. Kolloidal. Çözelti < 10-9 m Süspansiyon > 10-6 m Kolloid 10-9 m m
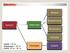 Aeresol Süspansiyon Karışım Heterojen Emülsiyon Kolloidal Çözelti < 10-9 m Süspansiyon > 10-6 m Kolloid 10-9 m - 10-6 m Homojen Çözelti Dağılan Faz Dağılma Fazı Kolloid Tipi katı katı,sıvı,gaz sol katı
Aeresol Süspansiyon Karışım Heterojen Emülsiyon Kolloidal Çözelti < 10-9 m Süspansiyon > 10-6 m Kolloid 10-9 m - 10-6 m Homojen Çözelti Dağılan Faz Dağılma Fazı Kolloid Tipi katı katı,sıvı,gaz sol katı
Genel Kimya 101-Lab (4.Hafta) Asit Baz Teorisi Suyun İyonlaşması ve ph Asit Baz İndikatörleri Asit Baz Titrasyonu Deneysel Kısım
 Genel Kimya 101-Lab (4.Hafta) Asit Baz Teorisi Suyun İyonlaşması ve ph Asit Baz İndikatörleri Asit Baz Titrasyonu Deneysel Kısım Asit Baz Teorisi Arrhenius Teorisi: Sulu çözeltlerine OH - iyonu bırakan
Genel Kimya 101-Lab (4.Hafta) Asit Baz Teorisi Suyun İyonlaşması ve ph Asit Baz İndikatörleri Asit Baz Titrasyonu Deneysel Kısım Asit Baz Teorisi Arrhenius Teorisi: Sulu çözeltlerine OH - iyonu bırakan
KIMYASAL DENGE. Dinamik Denge. Denge Sabiti Eşitliği. Denge Sabiti Eşitliği. Denge Sabiti Eşitliği. Denge Sabiti Eşitliği
 Dinamik Denge KIMYASAL DENGE COMU, Egitim Fakültesi www.sakipkahraman.wordpress.com Bir sıvının buhar basıncı denge konumuna bağlı bir özelliktir. Çözünen bir katının çözünürlüğü denge konumuna bağlı bir
Dinamik Denge KIMYASAL DENGE COMU, Egitim Fakültesi www.sakipkahraman.wordpress.com Bir sıvının buhar basıncı denge konumuna bağlı bir özelliktir. Çözünen bir katının çözünürlüğü denge konumuna bağlı bir
A A A A A KİMYA TESTİ. 4. Aynı periyotta bulunan X ve Y elementleri 5... C 3 2. X 2 6. CH mol XY gazı ile 4 mol Y 2 Ö Z G Ü N D E R S A N E
 KİMY TTİ 1. Bu testte 30 soru vardır. Testin tümü için verilen cevaplama süresi 45 dakikadır. 1. Yukarıda eşit hacimli iki kapta aynı koşullar altında bulunan gazlar aradaki musluk sabit sıcaklıkta açıldığında
KİMY TTİ 1. Bu testte 30 soru vardır. Testin tümü için verilen cevaplama süresi 45 dakikadır. 1. Yukarıda eşit hacimli iki kapta aynı koşullar altında bulunan gazlar aradaki musluk sabit sıcaklıkta açıldığında
ÇÖZELTİLER VE ÇÖZELTİ KONSANTRASYONLARI 3.1. Çözeltiler için kullanılan temel kavramlar
 1.10.2015. ÇÖZELTİLER VE ÇÖZELTİ KONSANTRASYONLARI.1. Çözeltiler için kullanılan temel kavramlar Homojen karışımlardır. Çözelti iki veya daha fazla maddenin birbiri içerisinde homojen olarak dağılmasından
1.10.2015. ÇÖZELTİLER VE ÇÖZELTİ KONSANTRASYONLARI.1. Çözeltiler için kullanılan temel kavramlar Homojen karışımlardır. Çözelti iki veya daha fazla maddenin birbiri içerisinde homojen olarak dağılmasından
KARIŞIMLARIN SINIFLANDIRILMASI HAZIRLAYAN FEHMİ GÜR
 IN SINIFLANDIRILMASI HAZIRLAYAN FEHMİ GÜR IN SINIFLANDIRILMASI Karışımlar hangi özelliklerine göre sınıflandırılır? Karışımların sınıflandırılmasında belirleyici olan faktörler nelerdir? Farklı maddelerin
IN SINIFLANDIRILMASI HAZIRLAYAN FEHMİ GÜR IN SINIFLANDIRILMASI Karışımlar hangi özelliklerine göre sınıflandırılır? Karışımların sınıflandırılmasında belirleyici olan faktörler nelerdir? Farklı maddelerin
ELEMENT Aynı tür atomlardan oluşmuş saf maddelere element denir. ELEMENTLERİN ÖZELLİKLERİ 1. Aynı tür atomlardan oluşurlar. 2. Saf ve homojendirler.
 SAF MADDE: Aynı cins atom ya da moleküllerden oluşmuş maddelere, saf medde ÖR. Elementler saf maddelerdir. Çünkü; hepsi aynı cins atomlardan oluşmuşlardır. Bileşikler saf maddelerdir. Çünkü; hepsi aynı
SAF MADDE: Aynı cins atom ya da moleküllerden oluşmuş maddelere, saf medde ÖR. Elementler saf maddelerdir. Çünkü; hepsi aynı cins atomlardan oluşmuşlardır. Bileşikler saf maddelerdir. Çünkü; hepsi aynı
FARMASÖTİK TEKNOLOJİ I «ÇÖZELTİLER»
 FARMASÖTİK TEKNOLOJİ I «ÇÖZELTİLER» Uygun bir çözücü içerisinde bir ya da birden fazla maddenin çözündüğü veya moleküler düzeyde disperse olduğu tektür (homojen: her tarafta aynı oranda çözünmüş veya dağılmış
FARMASÖTİK TEKNOLOJİ I «ÇÖZELTİLER» Uygun bir çözücü içerisinde bir ya da birden fazla maddenin çözündüğü veya moleküler düzeyde disperse olduğu tektür (homojen: her tarafta aynı oranda çözünmüş veya dağılmış
TAMPON ÇÖZELTİLER. Prof.Dr.Mustafa DEMİR M.DEMİR 09-TAMPON ÇÖZELTİLER 1
 TAMPON ÇÖZELTİLER Prof.Dr.Mustafa DEMİR M.DEMİR 09-TAMPON ÇÖZELTİLER 1 Tampon çözeltiler Kimyada belli ph larda çözelti hazırlamak ve bunu uzun süre kullanmak çok önemlidir. Ancak bu çözeltilerin saklanması
TAMPON ÇÖZELTİLER Prof.Dr.Mustafa DEMİR M.DEMİR 09-TAMPON ÇÖZELTİLER 1 Tampon çözeltiler Kimyada belli ph larda çözelti hazırlamak ve bunu uzun süre kullanmak çok önemlidir. Ancak bu çözeltilerin saklanması
KARIŞIM NEDİR? YANDAKİ RESİMDE GÖRÜLEN SALATA KARIŞIM MIDIR?
 KARIŞIMLAR KARIŞIM NEDİR? YANDAKİ RESİMDE GÖRÜLEN SALATA KARIŞIM MIDIR? Birden çok maddenin kimyasal bağ oluşturmadan bir arada bulunmasıyla meydana gelen maddelere karışım denir. Karışımlar görünümlerine
KARIŞIMLAR KARIŞIM NEDİR? YANDAKİ RESİMDE GÖRÜLEN SALATA KARIŞIM MIDIR? Birden çok maddenin kimyasal bağ oluşturmadan bir arada bulunmasıyla meydana gelen maddelere karışım denir. Karışımlar görünümlerine
KARIŞIMLARIN SINIFLANDIRILMASI
 IN SINIFLANDIRILMASI Doğadaki maddelerin çoğu saf halde bulunmaz. Çevremizde gördüğümüz maddeler genellikle karışım halindedir. Soluduğumuz hava, yediğimiz çikolata, kek, içtiğimiz meyve suyu, süt hatta
IN SINIFLANDIRILMASI Doğadaki maddelerin çoğu saf halde bulunmaz. Çevremizde gördüğümüz maddeler genellikle karışım halindedir. Soluduğumuz hava, yediğimiz çikolata, kek, içtiğimiz meyve suyu, süt hatta
ÖĞRETĐM TEKNOLOJĐSĐ VE MATERYAL GELĐŞTĐRME ÇÖZELTĐLER
 ÖĞRETĐM TEKNOLOJĐSĐ VE MATERYAL GELĐŞTĐRME ÇÖZELTĐLER Ders Sorumlusu: Prof. Dr. Đnci MORGĐL HAZIRLAYAN: NAZLI KIRCI ANKARA,2008 KONU ANLATIMI ÇÖZELTĐLER Đki ya da daha fazla kimyasal maddenin herhangi
ÖĞRETĐM TEKNOLOJĐSĐ VE MATERYAL GELĐŞTĐRME ÇÖZELTĐLER Ders Sorumlusu: Prof. Dr. Đnci MORGĐL HAZIRLAYAN: NAZLI KIRCI ANKARA,2008 KONU ANLATIMI ÇÖZELTĐLER Đki ya da daha fazla kimyasal maddenin herhangi
4. 25 o C de sulu çözeltilerin özellikleri ile ilgili olarak, 5. ph 7 olan sulu çözelti için,
 1. ( ) ( ) ( ( ) Yukarıda verilen asit baz tepkimesinde asit özellik gösteren maddeler hangileridir? A), 4. 25 o C de sulu çözeltilerin özellikleri ile ilgili olarak, I. ph poh ise OH 1x10 7 II. OH H ise
1. ( ) ( ) ( ( ) Yukarıda verilen asit baz tepkimesinde asit özellik gösteren maddeler hangileridir? A), 4. 25 o C de sulu çözeltilerin özellikleri ile ilgili olarak, I. ph poh ise OH 1x10 7 II. OH H ise
BASIN KİTAPÇIĞI ÖSYM
 BASIN KİTAPÇIĞI 00000000 AÇIKLAMA 1. Bu kitapç kta Lisans Yerle tirme S nav - Kimya Testi bulunmaktad r.. Bu test için verilen toplam cevaplama süresi 5 dakikadır.. Bu kitapç ktaki testlerde yer alan her
BASIN KİTAPÇIĞI 00000000 AÇIKLAMA 1. Bu kitapç kta Lisans Yerle tirme S nav - Kimya Testi bulunmaktad r.. Bu test için verilen toplam cevaplama süresi 5 dakikadır.. Bu kitapç ktaki testlerde yer alan her
TOPRAK ALKALİ METALLER ve BİLEŞİKLERİ
 Bölüm 4 TOPRAK ALKALİ METALLER ve BİLEŞİKLERİ Bu slaytlarda anlatılanlar sadece özet olup ayrıntılı bilgiler derste verilecektir. Be, Mg, Ca, Sr, Ba, Ra Magnezyum, kalsiyum, stronsiyum, baryum ve radyumdan
Bölüm 4 TOPRAK ALKALİ METALLER ve BİLEŞİKLERİ Bu slaytlarda anlatılanlar sadece özet olup ayrıntılı bilgiler derste verilecektir. Be, Mg, Ca, Sr, Ba, Ra Magnezyum, kalsiyum, stronsiyum, baryum ve radyumdan
ÇÖZELTİLERDE YÜZDELİK İFADELER. Ağırlıkça yüzde (% w/w)
 ÇÖZELTİ HAZIRLAMA İki veya daha çok maddenin çıplak gözle veya optik araçlarla yan yana fark edilememesi ve mekanik yollarla ayrılamaması sonucu oluşturdukları karışıma çözelti adı verilir. Anorganik kimyada,
ÇÖZELTİ HAZIRLAMA İki veya daha çok maddenin çıplak gözle veya optik araçlarla yan yana fark edilememesi ve mekanik yollarla ayrılamaması sonucu oluşturdukları karışıma çözelti adı verilir. Anorganik kimyada,
Çözelti iki veya daha fazla maddenin birbiri içerisinde homojen. olarak dağılmasından oluşan sistemlere denir.
 3. ÇÖZELTİLER VE ÇÖZELTİ KONSANTRASYONLARI Çözelti: Homojen karışımlardır. Çözelti iki veya daha fazla maddenin birbiri içerisinde homojen olarak dağılmasından oluşan sistemlere denir. Çözelti derişimi
3. ÇÖZELTİLER VE ÇÖZELTİ KONSANTRASYONLARI Çözelti: Homojen karışımlardır. Çözelti iki veya daha fazla maddenin birbiri içerisinde homojen olarak dağılmasından oluşan sistemlere denir. Çözelti derişimi
5.111 Ders Özeti #21 21.1
 5.111 Ders Özeti #21 21.1 AsitBaz Dengesi Bölüm 10 Okunsun Konular: Asit ve Bazların Sınıflandırılması, Suyun Öziyonlaşması, ph Fonksiyonları, Asit ve Baz Kuvvetleri, Zayıf Asit İçeren Dengeler. Asit ve
5.111 Ders Özeti #21 21.1 AsitBaz Dengesi Bölüm 10 Okunsun Konular: Asit ve Bazların Sınıflandırılması, Suyun Öziyonlaşması, ph Fonksiyonları, Asit ve Baz Kuvvetleri, Zayıf Asit İçeren Dengeler. Asit ve
MADDENİN AYIRT EDİCİ ÖZELLİKLERİ. Nazife ALTIN Bayburt Üniversitesi, Eğitim Fakültesi
 MADDENİN AYIRT EDİCİ ÖZELLİKLERİ Bayburt Üniversitesi, Eğitim Fakültesi www.nazifealtin.wordpress.com MADDENİN AYIRT EDİCİ ÖZELLİKLERİ Bir maddeyi diğerlerinden ayırmamıza ve ayırdığımız maddeyi tanımamıza
MADDENİN AYIRT EDİCİ ÖZELLİKLERİ Bayburt Üniversitesi, Eğitim Fakültesi www.nazifealtin.wordpress.com MADDENİN AYIRT EDİCİ ÖZELLİKLERİ Bir maddeyi diğerlerinden ayırmamıza ve ayırdığımız maddeyi tanımamıza
BÖLÜM. Kimyasal Türler Arası Etkileşimler. Zayıf Etkileşimler Test Kimyasal Tür Nedir? Test Zayıf Etkileşimler Test
 BÖLÜM 3 Kimyasal Türler Arası Etkileşimler Kimyasal Tür Nedir? Test - 1... 2 Lewis Sembolleri Test - 2...2 Kimyasal Türler Arası Etkileşimlerin Sınıflandırılması Test - 3...2 Kimyasal Türler Arası Etkileşimler
BÖLÜM 3 Kimyasal Türler Arası Etkileşimler Kimyasal Tür Nedir? Test - 1... 2 Lewis Sembolleri Test - 2...2 Kimyasal Türler Arası Etkileşimlerin Sınıflandırılması Test - 3...2 Kimyasal Türler Arası Etkileşimler
As +3, As +5, Sb +3, Sb +5, Sn +2, Cu +2, Hg +2, Pb +2, Mehmet Gumustas. Cd +2, Bi +3
 2. GRUP KATYONLARI As +3, As +5, Sb +3, Sb +5, Sn +2, Cu +2, Hg +2, Pb +2, Mehmet Gumustas Cd +2, Bi +3 2. Grup Katyonlar As +3, Sb +3, Sn +2, Cu +2, Hg +2, Pb +2, Cd +2, Bi +3 Bu grupta, asitli ortamda
2. GRUP KATYONLARI As +3, As +5, Sb +3, Sb +5, Sn +2, Cu +2, Hg +2, Pb +2, Mehmet Gumustas Cd +2, Bi +3 2. Grup Katyonlar As +3, Sb +3, Sn +2, Cu +2, Hg +2, Pb +2, Cd +2, Bi +3 Bu grupta, asitli ortamda
BÖLÜM. Asitler Bazlar ve Tuzlar. Asitler ve Bazları Tanıyalım Test Asitler ve Bazları Tanıyalım Test
 BÖLÜM 5 Asitler Bazlar ve Tuzlar Asitler ve Bazları Tanıyalım Test - 1... 2 Asitler ve Bazları Tanıyalım Test - 2... 2 Asitler ve Bazları Tanıyalım Test - 3... 2 Asitlerin / Bazların Tepkimeleri Test -
BÖLÜM 5 Asitler Bazlar ve Tuzlar Asitler ve Bazları Tanıyalım Test - 1... 2 Asitler ve Bazları Tanıyalım Test - 2... 2 Asitler ve Bazları Tanıyalım Test - 3... 2 Asitlerin / Bazların Tepkimeleri Test -
kpss Önce biz sorduk 50 Soruda SORU Güncellenmiş Yeni Baskı ÖABT KİMYA Tamamı Çözümlü ÇIKMIŞ SORULAR
 Önce biz sorduk kpss 2 0 1 8 50 Soruda 35 SORU Güncellenmiş Yeni Baskı ÖABT KİMYA 2013 2014 2015 2016 2017 Tamamı Çözümlü ÇIKMIŞ SORULAR Komisyon ÖABT KİMYA TAMAMI ÇÖZÜMLÜ ÇIKMIŞ SORULAR ISBN 9786053189121
Önce biz sorduk kpss 2 0 1 8 50 Soruda 35 SORU Güncellenmiş Yeni Baskı ÖABT KİMYA 2013 2014 2015 2016 2017 Tamamı Çözümlü ÇIKMIŞ SORULAR Komisyon ÖABT KİMYA TAMAMI ÇÖZÜMLÜ ÇIKMIŞ SORULAR ISBN 9786053189121
BÖLÜM 6 GRAVİMETRİK ANALİZ YÖNTEMLERİ
 BÖLÜM 6 GRAVİMETRİK ANALİZ YÖNTEMLERİ Kütle ölçülerek yapılan analizler gravimetrik analizler olarak bilinir. Çöktürme gravimetrisi Çözeltide analizi yapılacak madde bir reaktif ile çöktürülüp elde edilen
BÖLÜM 6 GRAVİMETRİK ANALİZ YÖNTEMLERİ Kütle ölçülerek yapılan analizler gravimetrik analizler olarak bilinir. Çöktürme gravimetrisi Çözeltide analizi yapılacak madde bir reaktif ile çöktürülüp elde edilen
ÇÖKTÜRME TİTRASYONLARI (Çöktürmeye Dayanan Volumetrik Analizler)
 ÇÖKTÜRME TİTRASYONLARI (Çöktürmeye Dayanan Volumetrik Analizler) Prof. Dr. Mustafa DEMİR http://web.adu.edu.tr/akademik/mdemir/ M.DEMİR(ADU) 2009-15-ÇÖKTÜRME TİTRASYONLARI 1 Çöktürme ile, gravimetrik analizlerin
ÇÖKTÜRME TİTRASYONLARI (Çöktürmeye Dayanan Volumetrik Analizler) Prof. Dr. Mustafa DEMİR http://web.adu.edu.tr/akademik/mdemir/ M.DEMİR(ADU) 2009-15-ÇÖKTÜRME TİTRASYONLARI 1 Çöktürme ile, gravimetrik analizlerin
ELEKTRO METALÜRJ BAHAR
 ELEKTRO METALÜRJ 2016-2017 BAHAR ANOT KATOT HÜCRE - ELEKTROL T Anot ve Katodun Enine Kesitleri Kenar Büyümesi Anod Anod Katod Katod Anod M + M + M + M + M + M + Hücrede Ak m Da Molarite = M = Çözünen
ELEKTRO METALÜRJ 2016-2017 BAHAR ANOT KATOT HÜCRE - ELEKTROL T Anot ve Katodun Enine Kesitleri Kenar Büyümesi Anod Anod Katod Katod Anod M + M + M + M + M + M + Hücrede Ak m Da Molarite = M = Çözünen
MÜH. BÖLÜMLERİ GENEL KİMYA-I DERSİ DÖNEM SONU SINAVI
 ERZURUM TEKNİK ÜNİVERSİTESİ ELEKTRİK-ELEKTRONİK ve İNŞAAT MÜH. BÖLÜMLERİ GENEL KİMYA-I DERSİ DÖNEM SONU SINAVI 08.01.015 Soru No 1 3 4 5 6 Toplam Puan Alınan Puan I II III IV Top Adı-Soyadı: Numarası:
ERZURUM TEKNİK ÜNİVERSİTESİ ELEKTRİK-ELEKTRONİK ve İNŞAAT MÜH. BÖLÜMLERİ GENEL KİMYA-I DERSİ DÖNEM SONU SINAVI 08.01.015 Soru No 1 3 4 5 6 Toplam Puan Alınan Puan I II III IV Top Adı-Soyadı: Numarası:
6. Aşağıdaki tablodan yararlanarak X maddesinin ne olduğunu (A, B,C? ) ön görünüz.
 1. Lavosier yasası nedir, açıklayınız. 2. C 2 H 4 + 3O 2 2CO 2 + 2 H 2 O tepkimesine göre 2,0 g etilenin yeterli miktarda oksijenle yanması sonucu oluşan ürünlerin toplam kütlesi nedir, hesaplayınız. 3.
1. Lavosier yasası nedir, açıklayınız. 2. C 2 H 4 + 3O 2 2CO 2 + 2 H 2 O tepkimesine göre 2,0 g etilenin yeterli miktarda oksijenle yanması sonucu oluşan ürünlerin toplam kütlesi nedir, hesaplayınız. 3.
12-B. 31. I. 4p II. 5d III. 6s
 -B.. 4p. 5d. 6s Baş kuantum sayısı n, açısal kuantum sayısı olmak üzere yukarıda verilen orbitallerin enerjilerinin karşılaştırılması hangisinde doğru verilmiştir? A) == B) >> C) >> D) >> E) >> ÖLÇME,
-B.. 4p. 5d. 6s Baş kuantum sayısı n, açısal kuantum sayısı olmak üzere yukarıda verilen orbitallerin enerjilerinin karşılaştırılması hangisinde doğru verilmiştir? A) == B) >> C) >> D) >> E) >> ÖLÇME,
KARADENİZ TEKNİK ÜNİVERSİTESİ FEN FAKÜLTESİ - KİMYA BÖLÜMÜ
 KARADENİZ TEKNİK ÜNİVERSİTESİ FEN FAKÜLTESİ - KİMYA BÖLÜMÜ TEMEL KİMYA LABORATUARI 2014 KİMYA LABORATUARLARINDA KULLANILAN MALZEMELER 2 BEHER ERLEN BALON JOJE CAM BALON MEZÜR BÜRET PİPET BAGET SOĞUTUCU
KARADENİZ TEKNİK ÜNİVERSİTESİ FEN FAKÜLTESİ - KİMYA BÖLÜMÜ TEMEL KİMYA LABORATUARI 2014 KİMYA LABORATUARLARINDA KULLANILAN MALZEMELER 2 BEHER ERLEN BALON JOJE CAM BALON MEZÜR BÜRET PİPET BAGET SOĞUTUCU
